Resumen
Los antibióticos (AB) son compuestos relativamente sencillos, producidos por bacterias u hongos que atacan específicamente a las bacterias. Interfieren en algún paso del metabolismo donde encuentran un blanco adecuado. Desde el descubrimiento de la penicilina, se han descubierto una docena de nuevos tipos de AB y optimizado o sintetizado cerca de una centena. Sin embargo, su eficacia se ha visto alterada por su uso excesivo o incorrecto, que conduce a la aparición y diseminación de bacterias resistentes (ABR). Estas ABR actúan impidiendo el ingreso, modificando o inactivando la droga, modificando al blanco, o activando los sistemas de enflujo. La gran capacidad de las bacterias de mutar y transferir genes, y la presencia de genes de resistencia esencialmente en plásmidos y transposones, contribuyen a su diseminación tanto entre bacterias emparentadas y/o patógenas como hacia bacterias no patógenas que son los reservorios de ABR. La sensación de haber perdido la batalla o de que las ganancias a futuro no son tan importantes, han disminuido el interés de los laboratorios farmacéuticos por buscar nuevos compuestos. Sin embargo desde la investigación básica aparecen nuevas alternativas ya sea utilizando la genómica como material de análisis de nuevos blancos, las defensas naturales del organismo huésped, u otros agentes olvidados como las bacterias predadoras y los fagos, ambos capaces de destruir bacterias.
Palabras clave: bacterias, antibióticos, resistencia
Antibiotics: yesterday, today and...tomorrow?
Summary
Antibiotics (AB) are relatively simple organic compounds produced by bacteria or fungi, killing prokaryotic cells. After the discovery of the first AB, penicillin, nearly a dozen of new and a hundred of synthetic compounds have been characterized. However, their therapeutic efficacy has dramatically decreased, essentially due to excessive or bad use, the emergence of antibiotic resistant bacteria (ABR), and their rapid spread among pathogenic or saprophytic bacteria. A few mechanisms are involved in ABR: uptake inhibition, drug modification or inactivation, target modification or enhancement of the multiefflux pumps. The great mutation capacity and high genetic transfer efficiency, essentially due to the presence of ABR on plasmids and transposons, contribute largely to disseminate these properties among related and unrelated bacteria.These difficulties and/or a bad economic perspective has lead industrial pharmaceutics to lose interest in research in this area. However, basic research making use of genomic analysis, host defense responses by the natural fighters and reconsideration of the destructive capacity of predatory bacteria and phages, re-open the way to pursue the combat.
Keywords: bacteria, antibiotics, resistance
Descubrimiento
|
|
| Figura 1. Placa de Petri con las colonias y el hongo penicillium |
Muchos descubrimientos tienen que ver con el azar y la suerte, aunque esta última requiere de la perspicacia del observador. Como dijo Louis Pasteur, y él sabia de lo que hablaba, “El azar solo favorece a los espíritus preparados”. El descubrimiento de los antibióticos no escapa a este axioma. Es a un joven escocés, Alexander Fleming, a quie se debe tal hazaña. La historia dice que investigaba en un laboratorio del hospital Saint Mary de Londres, cómo luchar contra enfermedades infecciosas y, ante todo, cómo eliminar bacterias patógenas. Ya había tenido su hora de azar-éxito observando que un cultivo de Staphylococcus aureus se había lisado al caérsele una lágrima. Así descubrió el rol antiséptico de la lisozima y su presencia en varios exudados naturales (lágrimas, mucosidades, etc...). Como este compuesto no resultó suficientemente activo como agente terapéutico, continuó sus ensayos y así fue como se encontraba en 1928 sembrando esas mismas bacterias en una caja de Petri, pero se fue de vacaciones y se las olvidó. A su regreso dos semanas más tarde la placa mostraba, además de las colonias esperables, la presencia de un hongo invasor. ¡Se había contaminado el experimento! En lugar de tirar su placa a la basura, se puso a observarla (Fig. 1). Alrededor del hongo ¡no había colonias! y sólo en los lugares más remotos al hongo estaban las colonias. Sospechó que del hongo debía difundir una sustancia inhibitoria. Así fue como se descubrió el primer antibiótico (AB), y se lo nombró Penicilina por el hongo Penicillium notatum (y luego P. chrysogenum), productores de dicho compuesto. Pero son los trabajos posteriores realizados por Howard Florey y Ernst Chain los que permitirán purificar la penicilina. Su enorme perfil terapéutico solo se pondrá en marcha durante la segunda guerra mundial. Fueron las necesidades de combatir las numerosas infecciones generadas por las mutilaciones las que impulsaron a la industria farmacéutica, principalmente en EE.UU (Eli Lilly, Pfizer Squibb, Merck, Lederle), y a las instituciones académicas a emprender el estudio de esta sustancia. Se habló del mayor milagro y se salvaron millones de vidas. En 1945, la Academia Sueca galardonó con el Premio Nobel de Medicina a sus tres importantes descubridores (Fleming, Chain y Florey) (Fig. 2).
 |
| Figura 2. Los Premios Nobel 1945 A. Fleming, E. Chain y H. Florey |
1940 - 1970 ha sido el periodo de oro del descubrimiento de nuevos antibióticos, ya sean naturales o sintéticos (Fig. 3). La desaceleración observada desde entonces (Fig. 4) se debe a varios factores, entre los cuales el más importante es la falta de inversión de la industria farmacéutica, desalentada por la rapidez con la cual cada nuevo antibiótico pierde su eficacia (ver resistencias a AB) (23 32). Los blancos de acción de los AB tienen que ver con la estructura y el metabolismo particular de las bacterias (células procariotas) que determinan su especificidad.
| ||||||||||||||||||||||||||||||
|
Figura 3. Antibióticos descubiertos entre 1935 y 2003
|
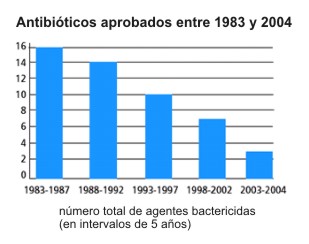 |
| Figura 4: Nuevos agentes bactericidas en el periodo 1983 y 2004 |
Cómo y cuándo actúan
Blanco de acción
Los AB se agrupan de acuerdo a su blanco de acción aunque no compartan una estructura química similar. Algunos actúan sobre la síntesis de las envolturas bacterianas, membrana o pared (beta-lactámicos, glicopéptidos, polimixinas…) otros sobre el proceso de replicación del ADN (quinolonas…), de transcripción (rifampicina..), el aparato de biosíntesis de proteínas (tetraciclinas, eritromicina, lincomicina, estreptomicina, cloranfenicol…) o sobre el metabolismo (sulfamidas) (fig.5). A su vez, para su actividad requieren que las bacterias se encuentren en división activa y que el antibiótico encuentre su blanco.
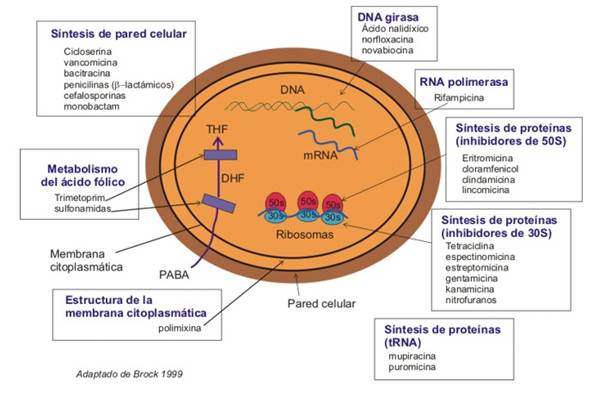
Figura 5. Tipos de AB y su blanco. (Brock 1999)
Pero las bacterias no se quedan quietas frente al AB y pueden desarrollan todo una serie de procesos (ver resistencias a AB) que le permiten inhibir su ingreso o excretarlo, modificar al AB para que pierda eficiencia o alterar el blanco. Durante mucho tiempo una alternativa desarrollada por la Industria farmacéutica ha sido la de ir modificando al AB cada vez que aparecía alguna de estos efectos adversos. Ese ha sido el caso de la penicilina y sus derivados β-lactámicos.
La penicilina y sus derivados: ping- pong entre antibióticos y resistencias bacterianas
La penicilina tiene un anillo β-lactámico (fig.6) gracias al cual compite con el sustrato natural de las enzimas PBPs (penicillin-binding proteins), responsables de la síntesis de la pared celular (peptidoglicano) (Fig.7). Su presencia hace que la nueva pared pierda el rol de contenedor de la estructura celular, lo que permite el ingreso descontrolado del agua y la lisis de la bacteria.
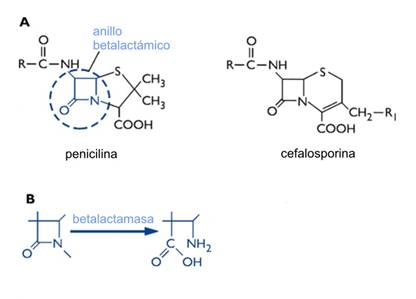 |
| Figura 6. |
En bacterias Gram positivas (como Staphylococus, Streptococus, Bacillus y Lactobacillus) la pared se encuentra inmediatamente accesible y constituye un blanco ideal, de ahí su eficacia Esto no ocurre en bacterias Gram negativas, donde la pared es mucho menor y se encuentra entre 2 membranas (Enterobacterias, Pseudomonas, Shigella, Serratia etc..) las que impiden su acceso al blanco (fig. 7).
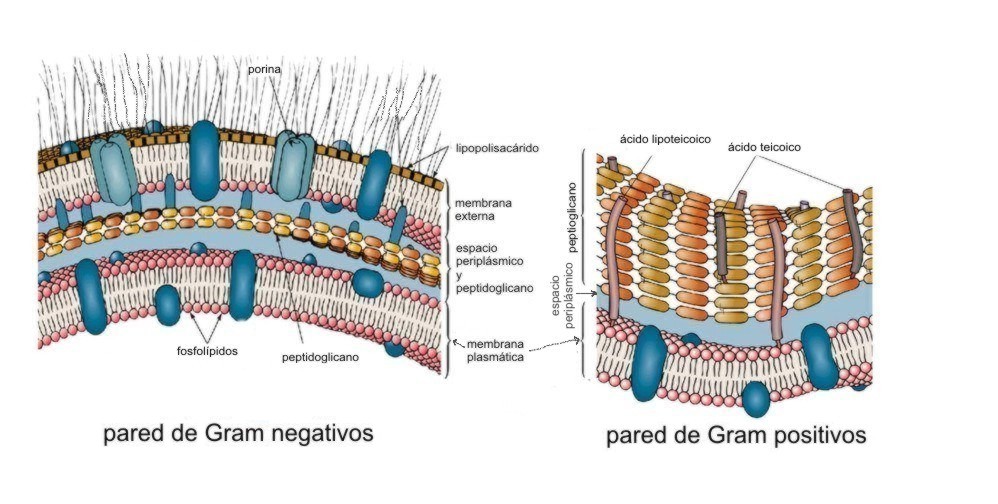 Figura 7. Estructura de las envolturas de Bacterias Gram + y Gram- |
Esta deficiencia se contrarrestó produciendo por síntesis química un derivado de la penicilina capaz de atravesar la capa lipídica y ser eficiente en infecciones producidas tanto por bacterias Gram+ como Gram- (Ej. cefalosporinas). Sin embargo, con su uso estos compuestos se tornaron ineficaces, pues algunas bacterias producen una enzima asociada a la pared (β-lactamasa) que rompe el anillo β-lactámico e inactiva la penicilina y sus derivados. De nuevo la industria química consiguió modificar la estructura del AB de forma tal que sea resistente a la actividad de las β-lactamasas (Ej Amoxicilina, ampicilina) o que la inactive (clindamicina). Esta última generación de AB también tiene la ventaja de soportar sin degradarse el tránsito por la acidez del estómago cuando se administran por vía oral.
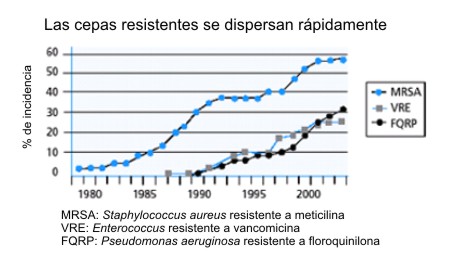
La historia no termina ahí, pues pronto se han puesto en evidencia las resistencias múltiples a antibióticos agenciadas por los sistemas eficientes de eflujo para arruinar el panorama. Es así como la vigencia de un antibiótico viene menguando en forma alarmante: mientras la penicilina G conservó su eficacia de 1944 a 1970 aproximadamente, los AB de última generación solo resisten unos cinco años o menos frente a la aparición de las temidas resistencias (Fig. 8). Como ejemplo, entre 1980-1990 la cantidad de infecciones con cepas de Neisseria gonorrhoeae resistentes a AB pasó de 0,1% al 10%. (3, 6, 17, 20, 21)
|
|
| Figura 8. Frecuencia de aparición de bacterias ABR en función del uso de AB. |
Las estructuras que impiden su camino al blanco
El acceso del AB a su sitio de acción no es un problema menor, pues como cualquier compuesto orgánico o iónico, excepto el agua, su acceso al blanco requiere sortear la barrera de las envolturas bacterianas. De ahí que muchos de los antibióticos más eficientes tienen su blanco en las envolturas. Este es el caso de las penicilinas (primer AB), vancomicina (AB de último recurso), y en la actualidad sigue siendo un polo importante de investigación. Pero además de las estructuras clásicas de envoltura descriptas, muchos microorganismos desarrollan envolturas adicionales (S-layers, cápsulas, biopelículas o matrices de exopolisacáridos, de ácidos mucólicos etc...) que impiden el ingreso de los AB. Estas estructuras a su vez no se desarrollan siempre en condiciones de laboratorio, pero si en los procesos infecciosos (Pseudomonas aeruginosa y fibrosis quística, Bacillus anthracis y ántrax etc…) y explican la ineficiencia de los AB en algunas situaciones.
Otro aspecto importante de los AB es que no todos terminan matando y lisando a las bacterias (acción bactericida y bacteriolítico como la penicilina), algunos sólo impiden su crecimiento (acción bacteriostática).
Esto permitió clasificar a los AB en dos grandes grupos:
| Bactericidas · Beta-lactámicos (Penicilinas y cefalosporinas) · Glicopéptidos (Vancomicina..) · Aminoglucósidos (Estreptomicina…) · Quinolonas (norfloxacino, ácido nalidixico...) · Polimixinas | Bacteriostáticos · Macrólidos (Grupo eritromicina) · Tetraciclinas · Cloranfenicol · Clindamicina, Lincomicina · Sulfamidas |
Por su eficiencia, muchos de los AB bacteriostáticos son paulatinamente eliminados, como en el caso del cloranfenicol.
AB y reacciones adversas
En principio los AB no interfieren con el normal desarrollo de las células u órganos animales. Sin embargo todos presentan cierta toxicidad. Se utilizan solo aquellos cuyo beneficio es superior a los inconvenientes que puedan ocasionar. Esta decisión se toma evaluando el índice de toxicidad selectiva.
Los antibióticos pueden provocar efectos adversos en el organismo, algunos de estos efectos son:
Alergia. Muchos antibióticos producen erupciones en la piel y otras manifestaciones de alergia (fiebre, artritis, etc), en un pequeño número de personas predispuestas. El choque anafiláctico es una reacción extrema que se observa tanto por el uso del AB por si mismo (penicilinas), como por el excipiente que lo acompañan.
Disbacteriosis. Al eliminar también bacterias "buenas" (de presencia deseable en el tubo digestivo) pueden producir dolor y picor en la boca y la lengua, diarrea, etc.
Sobrecrecimientos. Los antibióticos eliminan unas bacterias pero permiten que crezcan otras bacterias (se seleccionan las resistentes y/o se varía la composición normal de la flora) o predisponen el terreno para el crecimiento de hongos (caso de candidiasis).
Resistencias. Las bacterias intentan hacerse resistentes rápidamente a los antibióticos, y la administración continua o repetida de antibióticos para enfermedades menores favorece la aparición de estas resistencias.
Toxicidad. Los antibióticos pueden dañar los riñones, el hígado y el sistema nervioso, y producir alteraciones en los glóbulos de la sangre.
¿Qué son las resistencias y cómo se generan?
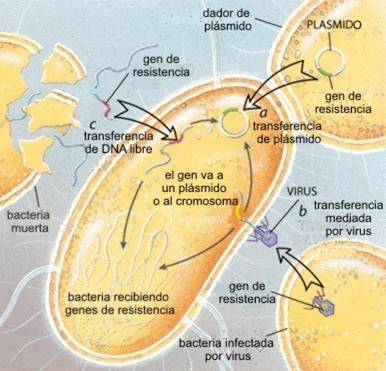
Las bacterias tienen una capacidad de división muy eficiente: dependiendo de las condiciones y del medio pueden dividirse en 20 min o hasta cada 100 días y más. En los procesos infecciosos, las bacterias se encuentran en activa división y se pueden contar hasta 109/ml. Estas dos condiciones hacen que se encuentren en el mejor escenario para que los mecanismos de variación genética operen eficientemente. Mutaciones en el genoma del huésped o en algún elemento asociado (plásmido, profago, etc.) eliminan la capacidad de transportar al AB, destruyen u modifican al AB, lo expulsan de la célula, o bien modifican al blanco (Fig 9). En cuanto a la posibilidad de transferir esta nueva capacidad, disponen de varios mecanismos (Fig. 10) entre los cuales los más conocidos son:
- la conjugación entre microorganismos emparentados o no, donde la presencia de plásmidos conjugativos promiscuos portadores de resistencias es un buen aliado
- la transduccción mediada por bacteriófagos
- la transformación donde la simple lisis libera el ADN que será captado por una bacteria receptora sin demasiadas restricciones, al menos a este nivel.
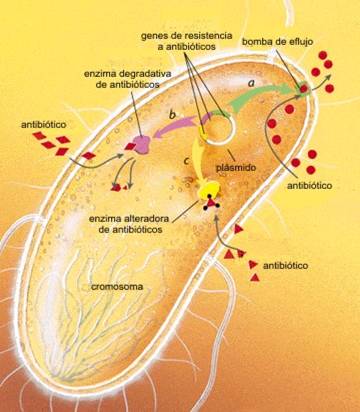 |
| Figura 9. Mecanismos de resistencia a los AB (Levy S. 1998) |
| - |
| Figura 10. Mecanismos de Transferencias de Resistencias a AB Levy S. 1998 |
Todos son utilizados y contribuyen a diseminar las ABR. Solo falta que el paciente los ayude. A los fines de que estos “individuos” sean seleccionados, bastará con que no se haya efectuado una destrucción total y rápida de las bacterias patógenas o de que se haya utilizado previamente en muchas ocasiones ese mismo AB.
Por otro lado, las resistencias a AB se encuentran con mucha frecuencia asociadas a estructuras como transpones y plásmidos o las dos a la vez. El primer plásmido de resistencia fue aislado en Japón en 1957 (fig. 11) y tiene todas estas características. Es importante remarcar que es un plásmido conjugativo promiscuo, capaz de transferirse entre especies no emparentadas; las resistencias se encuentran entre elementos transponible (IS o Tn) con lo cual saltaran la barrera de la recombinación homóloga y se pasearan dentro de bacterias muy diferentes. Estos elementos pueden además pasar de una ubicación inestable (plásmido ó fago) hacia una más estable (genoma bacteriano) (figura 10). Esto implica, además de estabilidad, poder adquirir las resistencias 100 a 1000 veces más eficientemente que por simple mutación y de paso adquirir varias a la vez. Estas estructuras se pueden trasladar con alta frecuencia entre sus congéneres, y lo que es peor, hacia otras bacterias no tan emparentadas como pueden ser los habitantes normales y necesarios de la flora intestinal. Estos se convierten en el reservorio de dichas resistencias e inocente partenaire listo para dotar al próximo patógeno invasor con una artillería de resistencias.
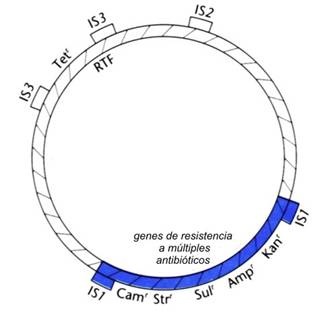 |
| Figura 11. Primer Plásmido multiresistente R1 o NR1, aislado en Japón en 1957 |
Por supuesto, plásmidos con similares características se aíslan permanentemente en cualquier huésped, y lo que es peor, de los hospitales, donde son un reservorio temido y son responsables de las famosas infecciones hospitalarias. Por si esto fuera poco, ahora se sospecha que el uso de los “simples desinfectantes” puede contribuir al aislamiento de bacterias resistentes, pero con un nuevo panorama: aumentan la eficiencia de los sistemas de detoxificación inespecíficos (bombas de eflujo multi valentes o multi efflux pump) (figura 12). Al mutar en un solo paso, pueden volverse más eficaces para que la bacteria se haga resistente a varios tipos y familias de antibióticos que podrían haber permitido una lucha más equitativa (1, 3, 10, 11, 24). Se podría llegar a pensar que el AB creó la resistencia, pero igual que el órgano no crea la función, las estructuras genéticas responsables ya se encuentran presentes y solo necesitan “adaptarse” y encontrase en el buen lugar en el buen momento. El AB solo sirve para seleccionar esos eventos y esas “raras” bacterias. De lugares aislados y donde no hubo contacto con antibióticos, se han aislado bacterias resistentes ¡incluso para AB sintéticos!.
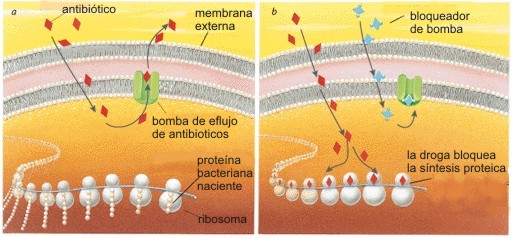 |
| Figura 12. Sistemas de eflujo del AB , Levy S. 1998 |
Uso y abuso
Las infecciones respiratorias por neumococos son una de las infecciones más comunes en pediatría; ya en 1960 empezaron a aparecer cepas resistentes a penicilina. En 1980 tanto España como Hungría y Sud-África dieron señales de alarma, pues en más del 50% de los casos las cepas eran resistentes. Así fue como en Hungría los pediatras decidieron evitar su administración. Entre 1983 y 1992 se observó que las resistencias a AB en las infecciones por Streptococcus pneumoniae bajaron del 50% al 34%. Este resultado indica que es posible revertir la situación, pues las cepas portadoras de resistencias utilizan parte de su energía al mantenimiento de dichas funciones, con lo cual su tasa de división es menor. En ausencia del AB se ven favorecidas aquellas que no mantienen esta propiedad, las capaces de crecer más rápidamente, o sea, las cepas sensibles al AB.
Actualmente se recetan aproximadamente 200 millones de antibióticos al año en Estados Unidos. Se estima que la mitad de estas prescripciones son inapropiadas debido a que el origen de la infección es viral. Además su uso ayuda a seleccionar a las resistentes de entre nuestras buenas bacterias saprofitas, con todo lo que ello implica para el futuro.
La aparición de cepas patógenas resistentes a AB es proporcional al uso de estos: entre 1980-1990 se utilizaron cerca de cuatro toneladas de gentamicina y resultó que cerca del 4% de las bacterias patógenas se volvieron resistentes. En ese mismo periodo se administró cerca de 100 toneladas de ampicilina y ahora el 70% de las infecciones perdieron su sensibilidad a dicho AB.
- El abuso de antimicrobianos en los hospitales como medida de profilaxis en las operaciones quirúrgicas está incrementando la resistencia antimicrobiana sin realmente beneficiar en muchos casos al paciente.
- Existe una tendencia a utilizar antibióticos de amplio espectro para combatir infecciones menos graves, lo que puede disminuir a posteriori la posibilidad de su uso en infecciones más virulentas y también reacciones tóxicas. Se siguen recetando las tetraciclinas para combatir infecciones que podrían ser tratadas más eficientemente con otros antibióticos menos tóxicos, y con un espectro más limitado.
- Muchos antibióticos se recetan sin identificar al microorganismo o realizar antibiogramas, incluso cuando dichos ensayos están claramente aconsejados.
- Normalmente se recetan los antibióticos más caros cuando otros más baratos son igual de efectivos. Dentro de los antibióticos más caros están las cefalosporinas y algunas tetraciclinas
- Muchas personas se automedican antibióticos. No es aconsejable dispensar antibióticos sin receta médica.
- Los tratamientos incompletos, donde el paciente abandona al AB por… Los efectos de esta práctica implican que se seleccionen ahora patógenos resistentes. Y solo hay que esperar que se multipliquen suficientemente para provocar los trastornos iniciales y de vuelta…
- Los animales de uso en nuestra alimentación han sido sospechados de constituir una fuente importante de bacterias resistentes. Se les administran AB tanto para el engorde (pollos, vacunos etc…) como para evitar que contraigan infecciones, con lo cual estos animales-alimento se convierten en portadores de bacterias resistentes a AB. Es así como se han podido detectar patrones plasmídicos con ABR en cepas aisladas de estos animales, cuyo perfil es muy semejante al que se encuentra en los humanos que los comieron. Esto indujo a que se analice la posibilidad de reglamentar su uso, como se muestra en el recuadro.
Extraido del INFORME DE LA REUNIÓN DE LA COMISIÓN DE NORMAS BIOLÓGICAS DE LA ORGANIZACIÓN MUNDIAL DE SANIDAD ANIMAL: París, 25–27 de enero de 2006
En varios países algunos antimicrobianos (por ejemplo, cloramfenicol, nitroimidazol y nitrofuran) están totalmente prohibidos para el uso veterinario y para el uso en animales de abasto con fines terapéuticos o para estimular el crecimiento. Algunos países han prohibido totalmente los antimicrobianos como estimuladores del crecimiento y los restringen a la utilización terapéutica o profiláctica.
En algunos casos muy específicos y cuando no hay alternativa, algunos Países Miembros de la OIE autorizan la utilización de antimicrobianos restringidos, por ejemplo, rifampicina combinada con eritromicina, que puede ser permitida para tratar la infección por Rhodococcus equi en los potros.
Cabe destacar que la importancia que tiene la utilización de los antimicrobianos depende del país.
-En agronomía, muchas enfermedades de los vegetales son de origen bacteriano y responden a los tratamientos por AB. Pero los inconvenientes son similares a los ya descritos: además, se agrega el inconveniente no solo de entrar en la cadena alimenticia pero también de quedar in situ y de poder alcanzar la capa acuífera. En este caso también se nota la preocupación de las autoridades competentes como se desprende del siguiente informe resumido:
Guía de principios en el uso de antibióticos según: National Health y Medical Research Council 24/3/2005
- minimizar su uso
- restringir a áreas cuya producción agrícola se vea afectada si no se usa
- cuando no haya otra alternativa
- evaluar y reducir los riesgos de sus uso en la aparición de ABR tanto en animales como humanos
- al AB debe degradarse rápidamente en el medio ambiente ya sea química o microbiológicamente
- no usar en casos innecesarios o cuando hay otras alternativas
- cuando la tasa de aparición de ABR es alta utilizar junto con otro AB a fin de disminuir la incidencia.
En ambos casos todo parece indicar que de momento solo hay alerta en cuanto a la necesidad de establecer regulaciones y que estas son muy dispares según los países. Las medidas dependerán del conocimiento de la “realidad” en cada país y de la presión que ejerzan las poblaciones en las instituciones responsables del control.
En cuanto a la introducción de genes de ABR en plantas transgénicas, hasta el momento hubo consenso y reglas internacionales para eliminar los genes de resistencia AB que sirvieron en los pasos de construcción.
- Necesidad de determinar el estado y forma de crecimiento del micro-organismo a combatir:
Los AB son más eficaces en bacterias dividiéndose activamente y menos eficaces en bacterias en reposo o formando quistes, cápsulas o biopelículas (ej.: fibrosis quística, placa dental etc… De ahí, la necesidad de determinar el estado de crecimiento in situ y de atravesar o eliminar la (s) barrera (s) con algún otro agente especifico.
Alerta -->la determinación de la susceptibilidad de un microorganismo al AB en el laboratorio puede ser muy diferente de su efectividad in vivo. Si es posible se debe corroborar su eficiencia en las condiciones más relacionadas al estado de crecimiento en el lugar de la infección.
¿Qué estrategias utilizar?
• Utilizar AB solo en caso necesario y asegurarse de que se trata de una infección bacteriana.
• Efectuar antibiogramas del microorganismo siempre que sea posible
• No interrumpir un tratamiento una vez iniciado.
• Evitar los AB de última generación a fin de resguardarlos para su uso en casos extremos
• Averiguar el estado de crecimiento del microorganismo (activo o estacionario, crecimiento planctónico versus biofilms, presencia de cápsulas, S-layers etc..)
• Evitar por un tiempo su uso a fin de eliminar la carga de bacterias resistentes
• Atención: Algunas toxinas son liberadas cuando se lisan las bacterias (ejemplo: botulismo). Esto implica que en esos casos el AB se debe manejar con suma precaución, y administrar junto con un una antitoxina.
Se ha observado presencia de daño tisular como consecuencia del tratamiento antibiótico, que provoca lisis bacteriana y exacerbación de la respuesta.
En el botulismo del lactante no deben administrarse antimicrobianos ya que la destrucción de las formas vegetativas a nivel intestinal provocan una liberación de toxina y empeora el cuadro
Nuevos compuestos, nuevos horizontes. La batalla continua
1- Compuestos de origen vegetal
Los antibacterianos de origen microbiológico parecen haber agotado sus posibilidades en esta lucha; sin embargo, desde las plantas o árboles, ya sean terrestres o acuáticas, se han identificado compuestos con diferentes actividades antibacterianas, antifúngicas, antivirales, anticancerígenas etc. que constituyen un importante reservorio. Distintos tipos de extractos y aceites han sido utilizados a lo largo de la historia en forma empírica y constituyen la base de numerosas terapias homeopáticas. Actualmente numerosos laboratorios de investigación se dedican a ellos y podrían ser fuente de novedosos antibacterianos (22, 25).
2- La Genómica permite diseñar nuevas estrategias
A partir del análisis de la secuencia genómica de las bacterias, no solo se puede intuir con cuántos genes y cuántas proteínas puede contar determinado microorganismo, sino también cuáles son esenciales para vivir, al menos, en condiciones de laboratorio. Así se puso en evidencia que muchos de los genes que tienen que ver con la síntesis de envolturas son esenciales y no tanto los genes regulatorios; que serían una exquisitez para no malgastar energía.
Del análisis de las proteínas esenciales y de su posible configuración (11, 13, 15, 27), se pueden “diseñar” nuevos antibióticos (11, 14, 18). Las envolturas siguen siendo el blanco preferido (21, 22). Ese ha sido también el blanco de un nuevo antibiótico recientemente caracterizado producido por Streptomyces platensis cuya novedad consiste en afectar la síntesis de los ácidos grasos que componen la membrana (34).
Otra alternativa evaluada por estudios recientes donde es importante conocer más de la genómica de la bacteria a eliminar, ha sido la de limitar la capacidad mutagénica interfiriendo con los genes responsables de sus mecanismos de reparación (6).
3- Péptidos animales, bacterias devoradoras de otras bacterias etc… ¿hacia nuevas formas de antibacterianos?
Defensinas, dermicinas, lisozima, lactoferrina (bactericida, antiviral y anti-inflamatorio inhibidor de formación de biopelículas en Pseudomonas), surfactinas etc. son proteínas, péptidos o lipopéptidos naturales que el organismo pone en funcionamiento para mantener a raya la multitud de posibles agentes infecciosos con los cuales debe convivir (12). Estos constituyen un campo a explorar. Algunos de ellos ya son conocidos y son considerados como posibles alternativas, pero requieren estudios más exhaustivos en cuanto a eficacia, espectro de acción, especificidad, toxicidad etc. (14, 26, 28, 30).
También algunas bacterias sintetizan péptidos o proteínas capaces de eliminar, por diferentes mecanismos, a sus semejantes (bacteriocinas). Estos compuestos son específicos y actúan en bacterias emparentadas con las productoras. Se utilizan esencialmente en la industria alimenticia, donde algunas especies bacterianas como los Lactobacilos, son requeridas por sus propiedades benéficas (probióticos, prebióticos) y donde se requiere eliminar otras especies no deseables en el alimento (9). Es del conocimiento de estos factores, y de su posible ampliación que pueden provenir nuevas alternativas. Estas constituyen un polo atractivo de investigación cuyas aplicaciones se vislumbran en un futuro próximo.
Otro nuevo polo de interés lo constituyen el grupo de bacterias depredadoras. Estas bacterias han sido durante mucho tiempo una curiosidad, pues son capaces de encontrar un huésped adecuado al que “fagocitan” y destruyen. Últimamente su actividad bactericida ha despertado gran interés, pues las bacterias embestidas al ser atacadas por múltiples vías no desarrollan resistencias. Además, estas depredadoras no comparten ninguna similitud genética con su huésped. Hasta el momento solo se conocen las que atacan a bacterias Gram negativas. Lo que las hace mas atractivas es la capacidad de atacar algunos patógenos como Pseudomonas aeruginosa, de difícil tratamiento, ya que suelen crecer dentro de una bio-película, pero ésta no constituye una barrera para las depredadoras, con lo cual serían buenos bactericidas ahí donde los AB fallan (16).
4- Fagos: los olvidados y re-descubiertos luchadores.
Los fagos o virus bacterianos destruyen a la bacteria que los hospedó después de haberse reproducido ampliamente. Esta propiedad condujo a varios microbiólogos a pensarlos como posibles bactericidas. Fue el canadiense Félix D´Herelle (el que les dió el nombre de bacteriofagos por “comen bacterias”) a quien se le debe el mérito de haber pensado en su utilidad y proponer usarlos como agentes terapéuticos (1930-40). La revolución que generó el uso de la penicilina y de los AB en general, así como la posición de algunos investigadores de peso y renombre como Gunther Stent (29), desalentaron continuar en Occidente con esta vía de estudios y desarrollo. Esto condujo a que durante casi 40 años sólo en los países del Este, y en particular en la URSS, se prosiguiera con ese campo terapéutico. Así se generó en los años 1930 en Tbilisi (Georgia) el primer centro donde llevar a cabo este proyecto, y solo en 1982 apareció en Canadá el “Félix d'Hérelle Reference Center for Bacterial Virus”. Actualmente la utilización de fagos es un campo en plena exploración en todo el mundo por diferentes motivos, tanto básicos como aplicables. Son una herramienta genética de fácil uso, no presentan toxicidad alguna, pueden ser útiles para insertar epitopos antigénicos en sus envolturas: Por otro lado son una muy buena alternativa a los AB: son específicos de especie, lisan las bacterias susceptibles en menos de 1hora, se pueden aplicar directamente en la piel o ingerir sin que se destruyan en el tubo digestivo (algunos reconstituyentes de flora intestinal los incluyen), aumentan su número en forma exponencial cuando encuentran a su blanco (amplificación del bactericida). Son pocos los restos celulares que quedan. Su inconveniente sigue siendo la liberación de toxinas por lisis, cuando ésta es el factor de virulencia. Pero todo es cuestión de rapidez (7, 8, 16, 19, 35)
Como podemos ver, queda abierto todo un panorama de posibilidades en cuanto a nuevas formas de antibacterianos. En este momento es del aprendizaje de los mecanismos de invasión y de respuesta del huésped que se vislumbran nuevas alternativas. Los fagos son una buena opción pero requieren mayor investigación. Igualmente tenemos que estar preparados a que nada en este campo es para siempre. Pero siempre es posible explorar nuevas direcciones que “casualmente” vienen de la mano del conocimiento.
No hay comentarios:
Publicar un comentario